Espaço para comunicar erros nesta postagem
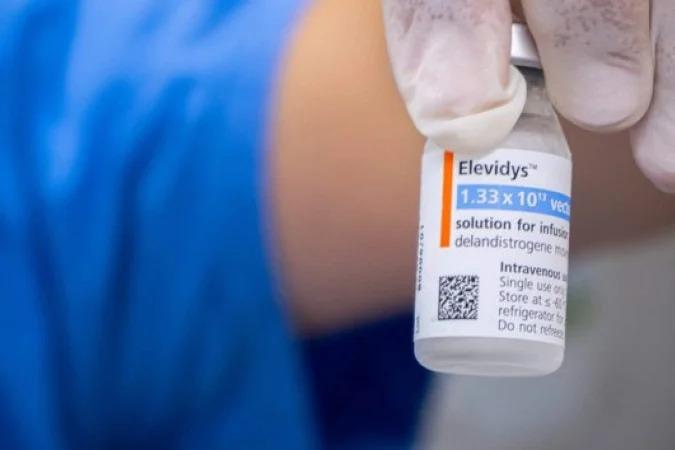
A Agência Nacional de Vigilância Sanitária (Anvisa) suspendeu, de forma temporária, a venda, distribuição e uso do medicamento Elevidys no Brasil. A medida foi tomada após a morte de uma criança brasileira que havia recebido a terapia genética, indicada para tratar distrofia muscular de Duchenne — uma doença rara e degenerativa. O remédio, desenvolvido pela farmacêutica Sarepta Therapeutics, pode custar até R$ 20 milhões por dose.
A decisão foi motivada por um alerta da FDA (Food and Drug Administration), agência reguladora dos Estados Unidos, que informou a ocorrência de três mortes relacionadas a terapias genéticas com a mesma tecnologia. Uma delas foi registrada no Brasil.
Responsável pela comercialização do produto no país, a Roche afirmou que, segundo avaliação médica, não há evidências de que a morte da criança esteja diretamente relacionada ao uso da Elevidys. A empresa também reforçou que, entre os cerca de 760 pacientes deambuladores (aqueles que ainda conseguem andar) que receberam a terapia, não há registro de óbitos associados ao tratamento.
A farmacêutica acrescentou que continua em diálogo com a Anvisa e autoridades sanitárias internacionais, e mantém sua posição de que os benefícios da Elevidys ainda superam os riscos, com base nos dados disponíveis até o momento.
A Anvisa, por sua vez, informou que todos os casos de morte relatados estavam associados a usos não autorizados do medicamento no Brasil. Desde dezembro de 2024, a Elevidys possui autorização excepcional e restrita no país: pode ser administrada apenas em crianças de 4 a 7 anos, que conseguem caminhar e possuem mutação confirmada no gene DMD.
Apesar disso, a suspensão foi adotada como uma medida preventiva, enquanto novas avaliações de segurança são conduzidas em conjunto com agências reguladoras internacionais.
Segundo comunicado da FDA divulgado na sexta-feira (25), a morte mais recente ocorreu em 7 de junho e envolveu uma criança de oito anos. A agência americana solicitou a suspensão voluntária da distribuição do medicamento até que sejam esclarecidas eventuais falhas de segurança. As outras duas mortes envolvem um adulto e outra criança.
De acordo com a FDA, os três óbitos foram causados por falência hepática aguda. Dois dos pacientes — crianças que não caminhavam — recebiam Elevidys para tratar a distrofia de Duchenne. O terceiro era um adulto com distrofia muscular de cinturas, participante de um estudo clínico com uma terapia experimental baseada no mesmo vetor viral (AAVrh74).
Em nota, a Sarepta Therapeutics reforçou que a segurança dos pacientes é sua prioridade e reiterou sua colaboração com as autoridades sanitárias. A empresa destacou ainda que Elevidys é, atualmente, a única terapia genética aprovada para a distrofia muscular de Duchenne.
Administrada em dose única por via intravenosa, a Elevidys atua sobre o gene defeituoso causador da distrofia muscular de Duchenne — condição hereditária rara, caracterizada por fraqueza muscular progressiva.
Em um desdobramento internacional, o Comitê de Medicamentos para Uso Humano (CHMP), da Agência Europeia de Medicamentos (EMA), recomendou que a Elevidys não receba autorização para comercialização na Europa. A Roche lamentou a decisão. O medicamento foi aprovado pela FDA em junho de 2023.

Publicado por:
Quentuchas Notícias
Quentuchas nasceu em 16 de janeiro de 2021, com o propósito de trazer sempre informações com qualidade, agilidade, em primeira mão de Erechim e mundo.
Saiba Mais












Comentários